Malattia di Alzheimer
La malattia di Alzheimer è una patologia neurodegenerativa cronica e progressiva, caratterizzata da un decorso lento, determinata dalla degenerazione e distruzione delle cellule nervose. E’ associata ad un’atrofia cerebrale e ad un basso livello di neurotrasmettitori, come l’acetilcolina, coinvolti nella trasmissione di un impulso da una cellula all’altra nelle aree cerebrali connesse alla memoria e ad altre funzioni cognitive; la malattia di Alzheimer è, infatti, la forma più comune di demenza senile, contraddistinta da un’alterazione delle funzioni cognitive superiori come la memoria, il ragionamento, il linguaggio, e mette a rischio la capacità di parlare e pensare; la malattia può, inoltre, causare stati di confusione, cambiamenti d’umore e disorientamento temporo-spaziale, fino a pregiudicare la capacità di svolgere le normali attività quotidiane e perdere completamente l’autosufficienza.
Introduzione
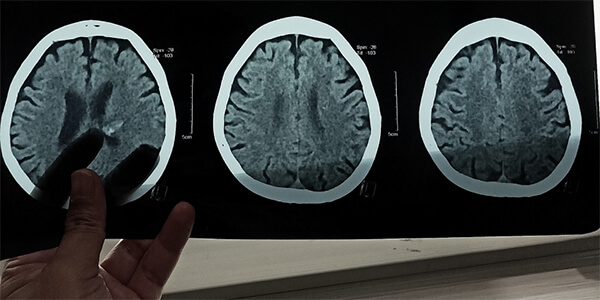
La malattia di Alzheimer è caratterizzata microscopicamente da due lesioni tipiche: le placche senili (placche amiloidi) in sede extracellulare, costituite dall’accumulo del peptide ß-Amiloide (Aß) e gli ammassi neurofibrillari intracellulari di proteina tau iperfosforilata. La ß-Amiloide è un frammento derivato dal taglio della proteina transmembrana APP (Amyloid Precursor Protein) ad opera di ß-secretasi, dal quale si generano frammenti di Aß, aventi diversa lunghezza: Aß40 e Aß42; in particolare quest’ultimo tende ad accumularsi in fibrille amiloidi, evidenziabili come placche senili, in aree cerebrali come l’ippocampo, l’amigdala e la neocorteccia. L’altra lesione tipica della malattia di Alzheimer è rappresentata dagli ammassi neurofibrillari, presenti in sede intraneuronale e costituiti principalmente da proteina tau fosforilata. La proteina Tau fa parte di una famiglia di proteine che sostiene la struttura del neurone e regola il trasporto delle sostanze nutritive, interagendo con i microtubuli (MBPs). Le placche senili e gli ammassi neurofibrillari ostacolano il trafficking cellulare, portando ad errori di comunicazione tra i neuroni, compromettendo il flusso di sostanze nutritive e, infine, con l’evolvere della malattia, conducendo a una grave perdita neuronale. Nella malattia di Alzheimer, a livello macroscopico, è evidenziabile atrofia cerebrale, in particolare nelle strutture del lobo temporale mediale (tra le quali l’ippocampo, l’amigdala e la corteccia entorinale) un ingrandimento dei solchi parietali e un ingrossamento delle cavità ventricolari, secondario alla perdita di parenchima.
Classificazione
Una prima importante distinzione può essere fatta tra forme “sporadiche” e forme famigliari.
Le forme più frequenti (circa il 90-95%) sono sporadiche, cioè si manifestano in un solo individuo in famiglia e non presentano famigliarità. Nelle forme famigliari (5-10% circa) sono colpiti dalla malattia più membri della stessa famiglia. Esse sono causate da un gene alterato che si trasmette alle generazioni successive; spesso hanno un esordio precoce: prima dei 65 anni.
Le forme famigliari, in generale, sono trasmesse con modalità di tipo ‘autosomico dominante” : ciò significa che il 50% dei figli del genitore portatore della mutazione ha la possibilità di ereditarla e di manifestare i sintomi in età adulta. Ad oggi sono stati identificati alcuni geni che, se mutati, possono causare la malattia: il gene della proteina amiloide (APP), il gene della presenilina-1 (PSEN1) ed il gene presenilina-2 (PSEN2). Recentemente alcuni studi hanno posto molta attenzione su una proteina plasmatica, l’APOE, che è coinvolta nel trasporto del colesterolo e che si lega alla proteina amiloide. Questa proteina esiste in tre forme; quella codificata dall’allele 4 (E4) è più frequente nelle persone affette da Alzheimer. La presenza del genotipo E4 aumenterebbe di circa tre volte il rischio di sviluppare la malattia; al contrario il genotipo APOE2 avrebbe invece un ruolo protettivo nei confronti dell’Alzheimer.
Epidemiologia
A causa dell’invecchiamento della popolazione, la demenza di Alzheimer rappresenta una patologia in continuo aumento e di grande interesse per i sistemi socio-sanitari, essendo una malattia altamente invalidante, a grande impatto sulle famiglie e sui servizi assistenziali. Da quanto riportato dall’ADI (Alzheimer’s Disease International) la demenza di Alzheimer rappresenta il 50-60% delle demenze, colpendo circa 24/28 milioni di persone nel mondo, con circa 5 milioni di nuovi malati ogni anno. In Europa la demenza di Alzheimer rappresenta il 54% di tutte le demenze, con una incidenza nella popolazione con più di 65 anni del 4,4%. Le donne risultano più colpite da questa patologia, con valori che vanno dallo 0,7% per la classe d’età 65-69 anni al 23,6% per le ultranovantenni; la percentuale per gli uomini risulta rispettivamente pari a 0,6% e a 17,6% nelle due classi di età. Secondo lo studio ILSA del CNR, in Italia la demenza interessa il 6,4% delle persone oltre i 65 anni.
Sintomi
La malattia di Alzheimer è caratterizzata da un andamento lento e progressivo, variabile da individuo ad individuo. Le manifestazioni sintomatologiche, con il progredire della malattia, sono sempre più gravi: la perdita di memoria è tale da indurre l’individuo a porre ripetutamente le stesse domande; i deficit cognitivi compromettono le capacità dell’individuo di seguire delle indicazioni, di orientarsi, di curare la propria persona nell’igiene e nella nutrizione, andando a compromettere significativamente la propria autonomia. La sintomatologia nella malattia di Alzheimer comprende:
Deficit mnesici: la perdita della memoria all’esordio della malattia si manifesta con lievi lacune per diventare progressivamente sempre più importante; il paziente è incapace di ricordare fatti recenti; per esempio, dimentica nomi, numeri di telefono, cosa ha mangiato, dove ha riposto un oggetto (amnesia anterograda).
Disorientamento temporale e spaziale: caratteristico è l’wandering cioè il vagare senza meta.
Deficit intellettivi: compromissione delle capacità di giudizio, ragionamento, risoluzione dei problemi.
Anomia: progressiva compromissione del linguaggio con difficoltà a “trovare la parola giusta” con frequenti pause, eloquio povero, frequenti frasi stereotipate.
Aprassia: difficoltà ad utilizzare correttamente gli oggetti e ad autogestire la propria quotidianità, come vestirsi, scrivere, utilizzare le chiavi.
Agnosia: difficoltà a riconoscere familiari ed amici, cibi o bevande.
Alessia e agrafia: incapacità di leggere e di scrivere.
Acalculia: incapacità di effettuare semplici operazioni matematiche.
Afasia: incapacità di comprendere il linguaggio parlato e incapacità di parlare. Disturbi comportamentali/cambiamenti del tono dell’umore (ansia, depressione, agitazione, paranoia, sospettosità, aggressività, apatia, inversione sonno-veglia, ecc.)
Incontinenza urinaria
Classificazione in stadi della malattia di Alzheimer – GDS – (scala di Barry Reisberg)
La scala più utilizzata per la stadiazione clinica della Malattia di Alzheimer è la Global Deterioration Scale (GDS). Questa scala è utilizzata per valutare la gravità del decadimento cognitivo e per monitorare nel tempo il decorso progressivo della Malattia di Alzheimer. La GDS individua 7 stadi distinti, a gravità crescente, di deterioramento cognitivo: da “nessun declino” a “declino molto severo”.
Stadio I: nessun declino delle funzioni cognitive. Difetto di memoria non riferito dal paziente, né riscontrato dal medico nell’indagine.
Stadio II: declino molto lieve delle funzioni cognitive. Il paziente riferisce difetti della memoria, più frequentemente:
-non ricorda dove vengono messi oggetti, o i nomi dei familiari
-nell’indagine il medico non riscontra prove oggettive di perdita di memoria
-nessuna lacuna sul lavoro o nelle situazioni sociali
-preoccupazione adeguata per i sintomi presenti.
Stadio III: declino lieve delle funzioni cognitive. Comparsa di lacune ben definite:
-il paziente si può perdere trovandosi in un luogo non familiare
-difficoltà a ricordare ciò che il paziente legge
-minor rendimento sul lavoro
-il paziente comincia a manifestare una certa rinuncia nelle attività giornaliere
-le persone vicine notano nel paziente difficoltà nel trovare le parole e ricordare i nomi
-Durante l’indagine del medico il paziente può manifestare mancanza di concentrazione, difetti di memoria associati ad ansietà lieve o moderata
Stadio IV: declino moderato delle funzioni cognitive. Durante l’indagine del medico si possono manifestare:
-ridotta conoscenza degli eventi attuali e recenti, difetti nella memoria di fatti riguardanti la storia personale, difetti di concentrazione e ridotta capacità di svolgere compiti complessi.
-Diminuite capacità nel viaggiare, nella gestione del denaro ecc.
-Insorgenza di meccanismi di “difesa” come la rinuncia nelle situazioni impegnative e il diniego.
-Ridotte risposte affettive.
Stadio V: declino moderatamente severo delle funzioni cognitive. Durante il colloquio con il medico il paziente:
-presenta difficoltà a ricordare elementi rilevanti come il proprio indirizzo o numero di telefono, difficoltà di concentrazione (per esempio contare all’indietro).
-comincia ad avere bisogno di assistenza
-manifesta disorientamento temporo-spaziale, difficoltà nel vestirsi, nella cura personale, nei pasti.
Stadio VI: declino severo delle funzioni cognitive.
-Il paziente risulta per lo più ignaro di tutti gli avvenimenti recenti e delle esperienze della propria vita, conservando solo qualche cognizione del proprio ambiente, dell’anno, della stagione ecc. Può presentare difficoltà nel contare e l’incapacità di prendere decisioni, associate a perdita di forza e di volontà.
-Il paziente necessita di assistenza nella vita quotidiana, durante viaggi o spostamenti in luoghi familiari.
-Il soggetto presenta disturbi della minzione, frequentemente incontinenza e cambiamenti emotivi e della personalità: comportamenti maniacali, ossessivi o ripetitivi, violenti, sintomi di ansietà e agitazione.
-Il paziente mantiene la capacità di distinguere le persone familiari da quelle non familiari.
Stadio VII: declino molto severo delle funzioni cognitive
-Perdita delle capacità verbali: il paziente si esprime solo con brontolii.
-Incontinenza urinaria.
-Perdita delle fondamentali capacità psicomotorie come camminare e mangiare.
-Necessità di assistenza continua per il mantenimento della cura della persona.
-Frequenti sintomi e segni neurologici.
Diagnosi
È fondamentale una diagnosi precoce; a tale proposito è fondamentale riconoscere i primi segni di decadimento cognitivo da riferire al proprio medico. Esistono dei “campanelli d’allarme” la cui identificazione, da parte del paziente e/o dei famigliari, risulta utile per il curante per poter identificare i primi segni di decadimento cognitivo; questi segnali sono stati pubblicati dall’American Alzheimer Association e sono:
1. Perdita di memoria tale da interferire con la capacita’ lavorativa e mandare in confusione.
2. Difficolta’ nel fare le cose di tutti i giorni: per esempio cucinare e poi dimenticarsi di averlo fatto e servito.
3. Difficoltà a trovare le parole giuste.
4. Difficoltà nel senso dell’orientamento, perdere la strada di casa.
5. Vestirsi in modo inadeguato: indumenti sovrapposti, uscire a fare la spesa in accapatoio.
6. Difficolta’ a riconoscere i numeri o a fare dei calcoli.
7. Riporre oggetti nei posti sbagliati o strani.
8. Cambiamenti improvvisi ed immotivati di umore.
9. Cambiamento del carattere: da tranquillo a sospettoso e irascibile.
10. Perdita progressiva di interessi e spirito di iniziativa.
Dopo aver raccolto l’anamnesi accurata dal paziente e dai famigliari, nel sospetto di malattia di Alzheimer il medico curante potrà indirizzare il paziente verso un centro specialistico UVA (unità di Valutazione Alzheimer) dove il paziente sarà sottoposto ad un percorso diagnostico-terapeutico, che comprende la raccolta dei segni clinici riscontrati e una valutazione delle funzioni cognitive utilizzando dei test riconosciuti a livello internazionale. Uno dei test più utilizzati è l’MMSE (Mini Mental State Examination). Il Mini Mental State Examination (MMSE), sviluppato da Folstein ed al. nel 1975, è un test largamente utilizzato a livello internazionale per lo screening generale del funzionamento cognitivo globale. E’ un test composto da 11 domande (items), inerenti ad una specifica funzione cognitiva; il test viene utilizzato sia per lo screening del decadimento cognitivo, sia per seguire un paziente nel tempo. -I primi due items verificano la capacità del paziente di orientamento nel tempo e nello spazio, mediante una serie di domande relative alla data del giorno e al luogo in cui viene effettuato il test. -Vengono poi indagati i due tipi di memoria: a breve termine, chiedendo al paziente di ripetere tre parole appena pronunciate dall’esaminatore; memoria intenzionale, richiedendo successivamente di ripetere le stesse parole pronunciate prima. -Si valuta la capacità di calcolo e attenzione chiedendo di eseguire una sottrazione in serie e di ripetere una parola al contrario, lettera dopo lettera. -La capacità di denominazione viene studiata mostrando al paziente degli oggetti e chiedendo di denominarli; per valutare la capacità di ripetere del paziente gli si chiede di ripetere una frase appena ascoltata. -La comprensione del linguaggio viene indagata facendo eseguire al paziente un ordine, sia su comando orale che scritto. -La capacità di scrivere una frase di senso compiuto è indagata invitando il paziente a scrivere una frase di senso compiuto. -L’abilità prassico costruttiva si valuta invitando il paziente a copiare un disegno composto da due pentagoni, che si intersecano in due lati consecutivi formando un quadrilatero.
Il punteggio totale, dato dalla somma dei punteggi che il paziente ha ottenuto per ciascun item, può andare da un minimo di 0 (massimo deficit cognitivo) ad un massimo di 30 (nessun deficit cognitivo). Il punteggio soglia è 23-24; la maggior parte delle persone anziane non dementi ottiene punteggi raramente inferiori a 24. Le indagini di laboratorio prescritte potranno comprendere: emocromo, elettroliti, glicemia, funzionalità renale ed epatica, vitamina B12 e folati. Eventuali: sierologia per la lue, test genetici (mutazioni APP e preseniline, genotipizzazione APOE), marcatori biologici liquorali (Abeta, proteina tau e fosfo-tau). Le indagini strumentali potranno comprendere l’RMN (Risonanza Magnetica Nucleare) o indagini più specifiche di neuroimaging funzionale, come la tomografia a emissione di fotone singolo (SPECT) e la tomografia ad emissione di positroni (PET).
Terapia
Terapia farmacologica
La terapia utilizzata nel trattamento della malattia di Alzheimer utilizza farmaci sintomatici, i quali hanno lo scopo di rallentare le manifestazioni cliniche, non essendo ancora noti farmaci che curano la malattia; la prescrizione medica sarà il più possibile personalizzata, in base allo stadio della malattia di Alzheimer e al trattamento degli eventuali disturbi di comportamento associati.
Le categorie di farmaci antidementigeni nell’Alzheimer sono: – inibitori delle colinesterasi; – dopaminoagonisti;
Altri trattamenti
Possono risultare utili nel trattamento del paziente affetto da malattia di Alzheimer quegli interventi che agiscono sulle sfera cognitiva, comportamentale, relazionale ed emotiva, con l’obiettivo di migliorare la qualità di vita del paziente, ridurre la sua disabilità, cercando di rallentare il decorso della malattia e potenziando le sue residue capacità intellettive, sensoriali ed affettive. Per raggiungere l’obiettivo sarà fondamentale il ruolo della famiglia, il cui coinvolgimento risulta necessario, non solo come sostegno affettivo e psicologico, ma anche come parte integrante di un percorso terapeutico, per affrontare una malattia inesorabilmente progressiva ed invalidante. La riabilitazione cognitiva potrà essere effettuata con varie tecniche: dalla terapia occupazionale, alla terapia di riattivazione globale, alla musicoterapia. Terapia occupazionale: ha come obiettivo quello di cercare di risolvere problemi pratici che si possono incontrare nella vita quotidiana; il terapista occupazionale suggerirà ausili per agevolare le attività della vita quotidiana, istruirà anche il caregiver. Terapia di riattivazione globale: ha come scopo quello di stimolare la memoria del paziente, attraverso argomenti sia del passato che attuali, e di rimotivarlo attraverso la discussione di argomenti legati alla sua vita attuale. Musicoterapia: ha lo scopo di promuovere la comunicazione, le relazioni e l’apprendimento, attraverso l’utilizzo di elementi sonoro-musicali. In linea generale è importante mantenere inalterato il luogo in cui vive il paziente (casa, mobilio) in modo da favorirne l’orientamento spaziale, mettendo nel contempo in sicurezza tutti quegli ambienti (cucina, bagno,..) che possono rappresentare un pericolo per la persona malata.
Prevenzione
E’ importante “mantenere in forma” il cervello; a tale proposito l’Alzheimer’s Association (importante associazione degli USA) suggerisce alcune regole:
– prevenire costantemente malattie cardiache, diabete, ipertensione e ictus (fattori che possono aumentare il rischio di Alzheimer);
– tenere nella normalità peso, glicemia e colesterolo;
– assumere una dieta povera di grassi e ricca di antiossidanti. A tale proposito sembra che le verdure e i frutti di colore scuro (ricchi di antiossidanti protettivi, responsabili del loro colore acceso) possano essere un aiuto per il mantenimento dell’efficacia cognitiva; tra le prime ci sono la rucola, il cavolo nero, i ravanelli, i cavolini di Bruxelles, il cavolo cinese, la rapa, la melanzana, il peperone, gli spinaci e la cipolla. Per quanto riguarda la frutta: mirtilli, lamponi, ciliegie, more, prugne, uva, arance e fragole.
– Svolgere attività fisica, come camminare per 30 minuti al giorno: aumenta l’ossigenazione al cervello.
– Mantenere il cervello attivo e impegnato aumenta la sua vitalità, quindi è importante leggere, scrivere, giocare, imparare cose nuove, fare cruciverba.
– Avere rapporti sociali che occupino il tempo libero, con attività che richiedono sforzo fisico e mentale: socializzare, conversare, fare volontariato, frequentare un circolo, ritornare sui banchi di scuola. –
Evitare i traumi: usare il casco se si va in bicicletta e diminuire i rischi per le cadute.
– Non fumare, non usare droghe e limitare il consumo di alcolici.

Ci impegniamo ogni giorno per garantire l'accessibilità a farmaci di alta qualità.
Scopri di più su DOC
